Si je vous demande la différence précise entre un « produit pharmaceutique » et un « médicament », sauriez-vous répondre sans hésiter ? Beaucoup d’entre nous utilisent ces termes de façon interchangeable, pourtant la réglementation algérienne les distingue avec une grande rigueur.
Un « médicament » n’est en fait qu’UNE des catégories de « produits pharmaceutiques ».
Imaginez : un vaccin, une matière première, un gaz médical et une préparation magistrale. Qu’ont-ils en commun ? Ils sont tous des « produits pharmaceutiques ». Mais sont-ils tous des « médicaments » au sens strict ? Pas exactement.
Ces nuances sont clairement définies dans la loi n° 18-11 relative à la santé, et elles structurent tout notre écosystème sanitaire.
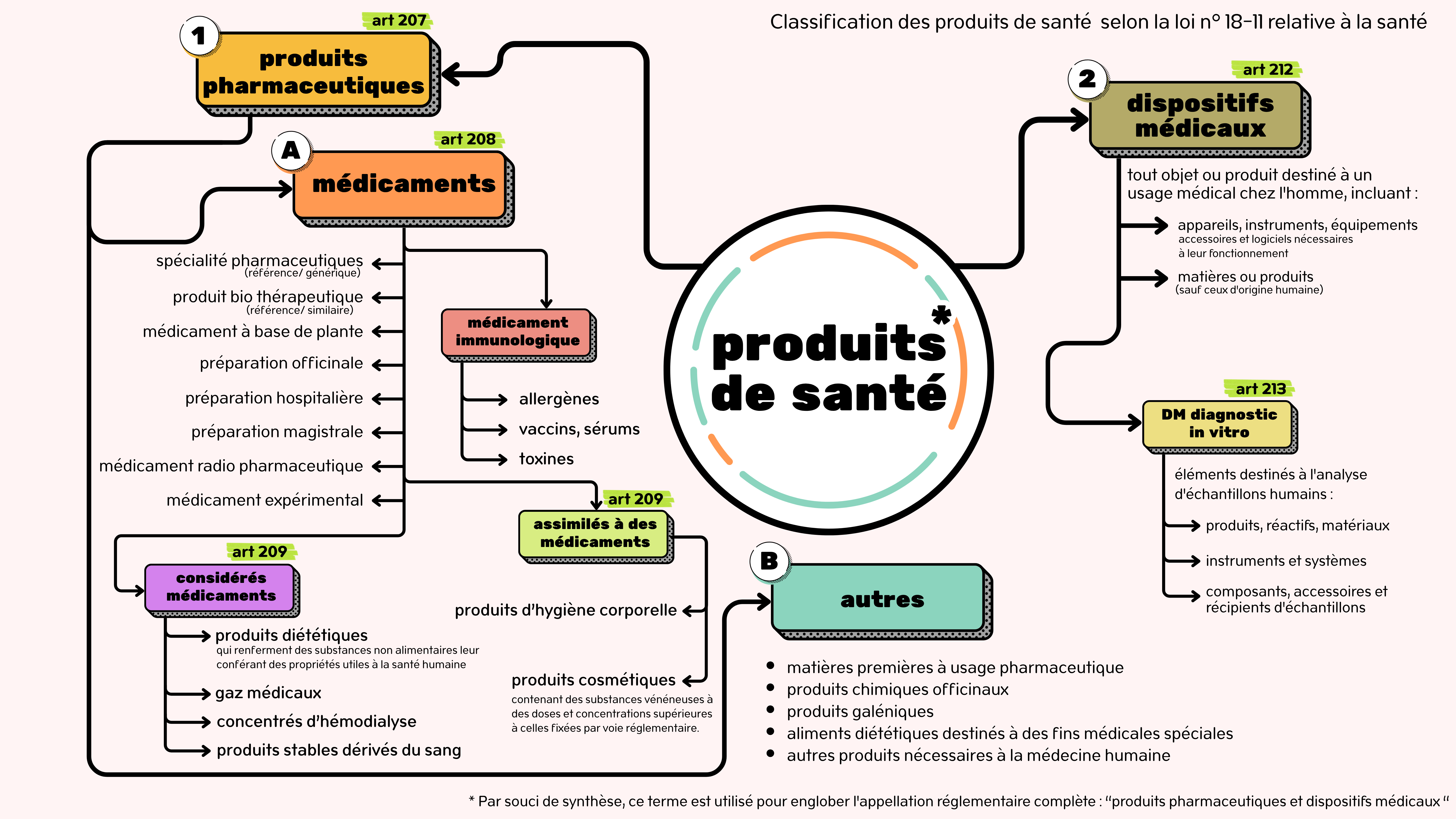
Pour synthétiser, je vous propose une cartographie visuelle organisée autour du terme générique « produits de santé » (employé ici par souci de clarté. La loi, elle, utilise l’intitulé : « produits pharmaceutiques et dispositifs médicaux »).
Le schéma s’articule donc autour de ces deux pôles légaux :
1. Les produits pharmaceutiques (Art. 207) : C’est la famille la plus vaste. Elle ne se limite pas aux médicaments (spécialités, génériques, préparations…), mais englobe aussi :
– Les produits considérés comme médicaments (gaz médicaux, produits stables dérivés du sang…).
– Les produits assimilés à des médicaments (certains cosmétiques contenant des substances spécifiques).
– Les autres produits nécessaires à la médecine (matières premières, aliments diététiques destinés à des fins médicales spéciales…).
2. Les dispositifs médicaux (Art. 212) : Cette branche couvre tout le matériel destiné à un usage médical, des instruments et équipements jusqu’aux logiciels. Elle comprend aussi la sous-catégorie des dispositifs médicaux de diagnostic in vitro (réactifs, instruments d’analyse…).
Comprendre cette taxonomie est important. Elle détermine le statut d’un produit, son circuit d’autorisation, de distribution et de contrôle. Pour les industriels, les pharmaciens qu’ils soient réglementaires ou autres, les juristes ou les ingénieurs biomédicaux, c’est la base pour garantir la conformité et la sécurité des produits mis à la disposition des patients.